Слушнете дискусија на експерти за натрим оксид инспирирани од нашите истраувања за NaOH
Галерија
Подкаст за хемијата на NaOH.
Инфографик за хемијата на NaOH.
Разбирање на натриум хидроксид (NaOH)
Разбирање на натриум хидроксид (NaOH)
Истражете ги основните аспекти на натриум хидроксид, од неговата структура и физички својства до неговите клучни хемиски реакции. Дознајте за неговото индустриско производство, различните апликации и основните безбедносни мерки. Сеопфатен преглед за сите заинтересирани за оваа витална хемикалија.
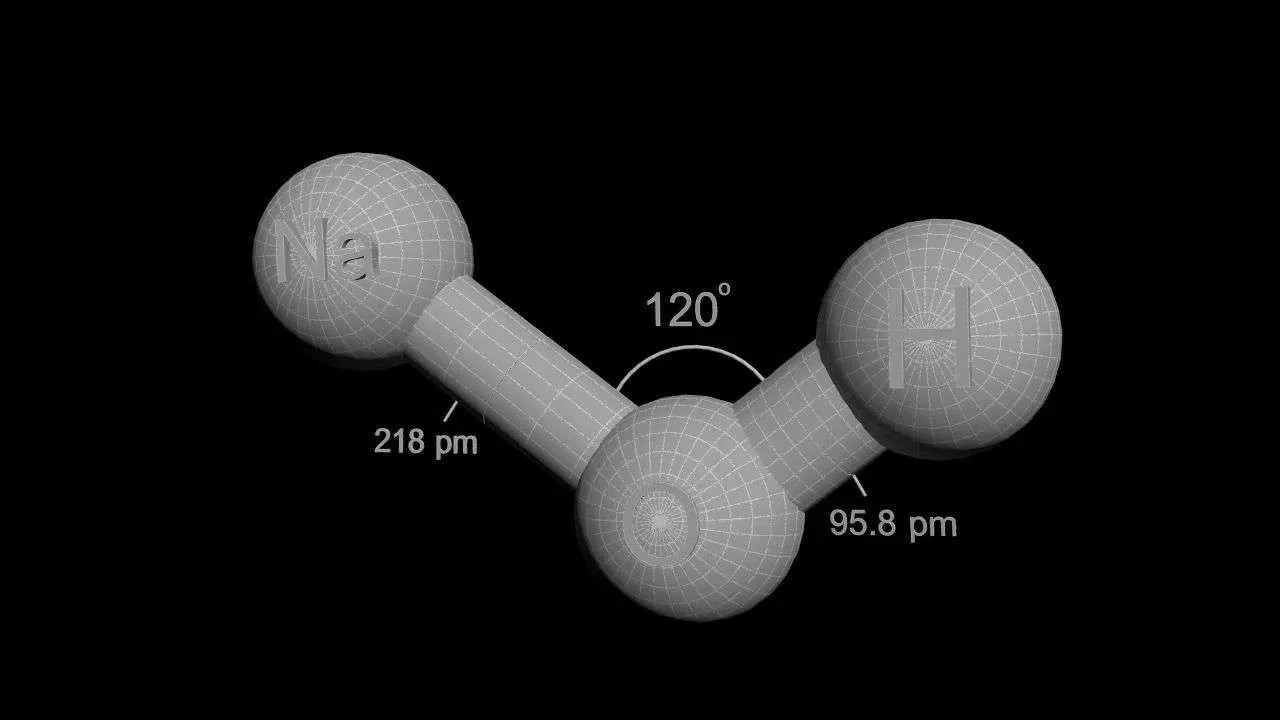
Натриум хидроксид (NaOH): Својства и индустриски апликации
Што е NaOH и неговата структура
Натриум хидроксид, познат како NaOH, е многу важна хемиска супстанција во хемијата и индустријата. Тоа е неорганско соединение кое се појавува како бела цврста материја и е составено од атоми на натриум (Na), кислород (O) и водород (H). Структурата на NaOH се состои од натриумови јони (Na⁺) и хидроксидни јони (OH⁻), што го прави силна база поради присуството на хидроксидниот јон. Оваа јонска структура му овозможува лесно да се дисоцира во вода, ослободувајќи хидроксидни јони кои се одговорни за неговите базни својства.
Физички својства на NaOH
NaOH е бела, без мирис и силно корозивна цврста материја која лесно апсорбира влага од воздухот, односно е хигроскопна. Има точка на топење од 318°C и точка на вриење од 1.388°C. Во цврста состојба најчесто се наоѓа во форма на пелети, лушпи или гранули. Кога се раствора во вода, создава силно алкален раствор, поради што е широко применуван во различни хемиски процеси. Неговата голема растворливост во вода и силната базност го прават важно соединение во многу индустриски примени.
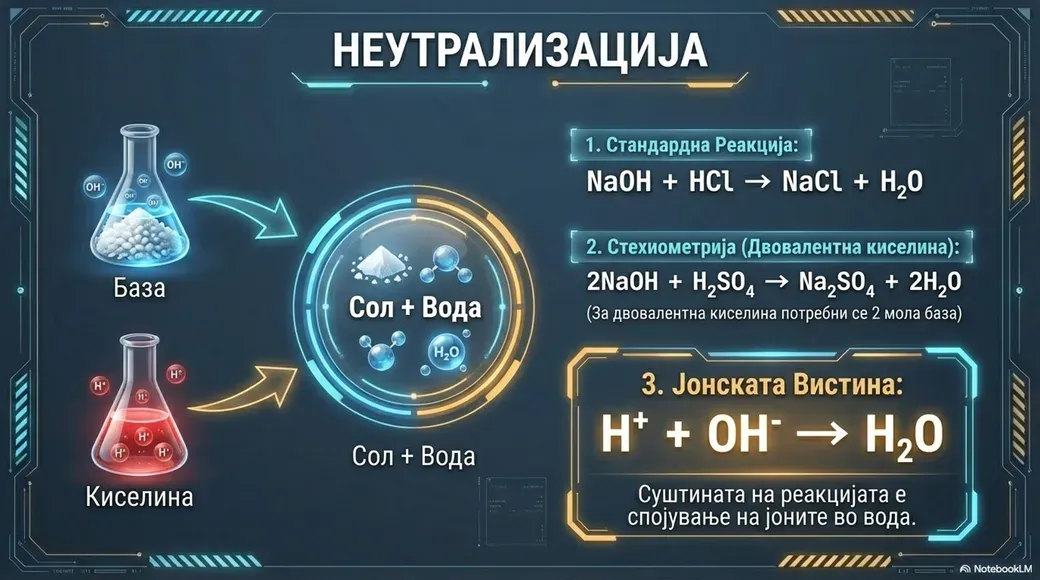
Хемиски својства и реакции
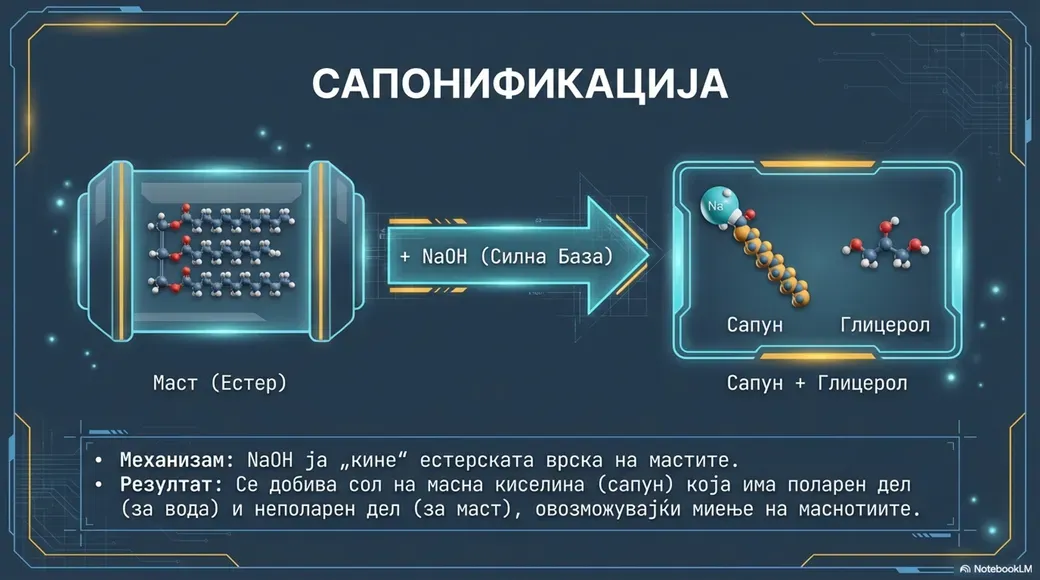
Како силна база, натриум хидроксид реагира со киселини во реакции на неутрализација при што се добиваат вода и соли. На пример, реагира со хлороводородна киселина (HCl) при што се создава натриум хлорид (NaCl) и вода (H₂O). Исто така реагира со киселински оксиди и амфотерни метали, што ја покажува неговата разновидност во хемиските процеси. Соединението учествува и во реакцијата на сапонификација, каде што реагира со масти и масла при што се добива сапун и глицерол – процес кој е основа на индустријата за производство на сапун.
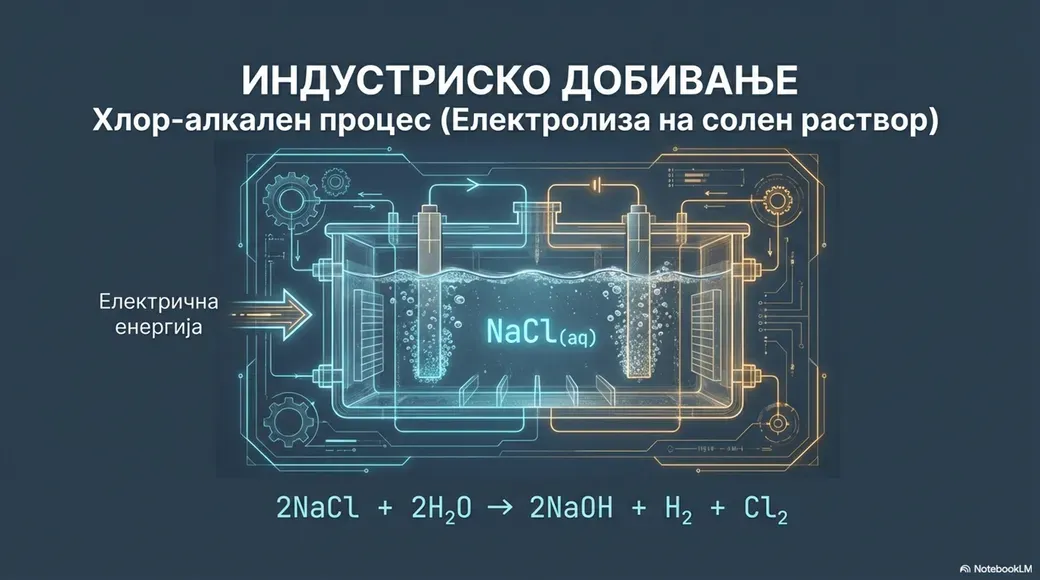
Индустриско добивање на NaOH
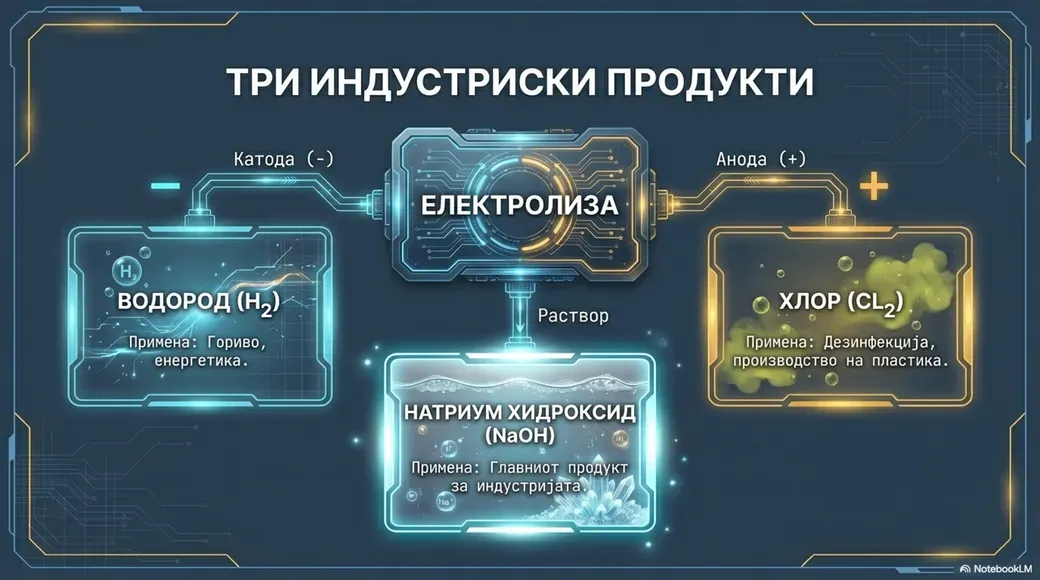
Главниот индустриски начин за добивање на натриум хидроксид е преку електролиза на саламура (раствор на кујнска сол во вода) во процес познат како хлор-алкален процес. Во овој процес се пропушта електрична струја низ растворот, при што се добиваат хлорен гас, водороден гас и натриум хидроксид. Процесот внимателно се контролира за да се обезбеди чистота и квалитет на произведениот NaOH, со што станува погоден за различни комерцијални и индустриски намени.
Примена и безбедност
NaOH широко се користи во различни индустрии, вклучувајќи хемиско производство, производство на хартија, третман на вода и производство на сапуни. Неговата способност да неутрализира киселини и да разградува органски материи го прави незаменлив во средствата за чистење и индустриските процеси.
Меѓутоа, поради неговата силна корозивност, NaOH може да предизвика сериозни изгореници при контакт со кожа или очи, па затоа при работа со него задолжително се користи заштитна опрема како ракавици и заштитни очила.